[대한식품의약신문=김재하 기자] 식품의약품안전처(처장 김강립)는 국내 개발 코로나19 백신 ‘IN-B009주’(에이치케이이노엔(주))의 안전성과 면역원성을 평가하기 위한 임상 1상 시험 계획을 7월 22일 승인했다.
이번 승인으로 국내에서 코로나19 관련해 임상시험을 진행하고 있는 의약품은 백신 10개, 치료제 13개(11개 성분) 등 총 23개 제품이다.
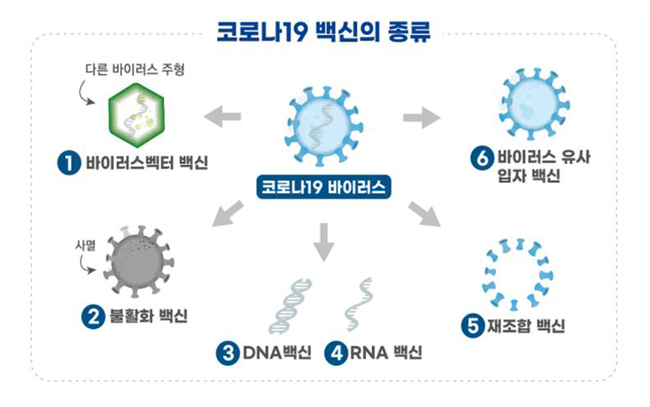
‘IN-B009주’는 코로나19 바이러스의 ‘표면항원 단백질’을 유전자 재조합 기술로 만든 ‘재조합 백신’이다.
특히 이번에 승인받은 백신은 표면항원 단백질의 N-말단 부위에 세포 투과 펩타이드(Cell Penetrating Peptide, CPP)를 추가로 발현시켜 세포 내로 단백질이 잘 전달될 수 있도록 개발됐다.
참고로 해외에서도 미국 노바백스社(3상) 등이 유전자재조합 기술을 이용한 코로나19 백신의 임상시험을 진행하고 있다.
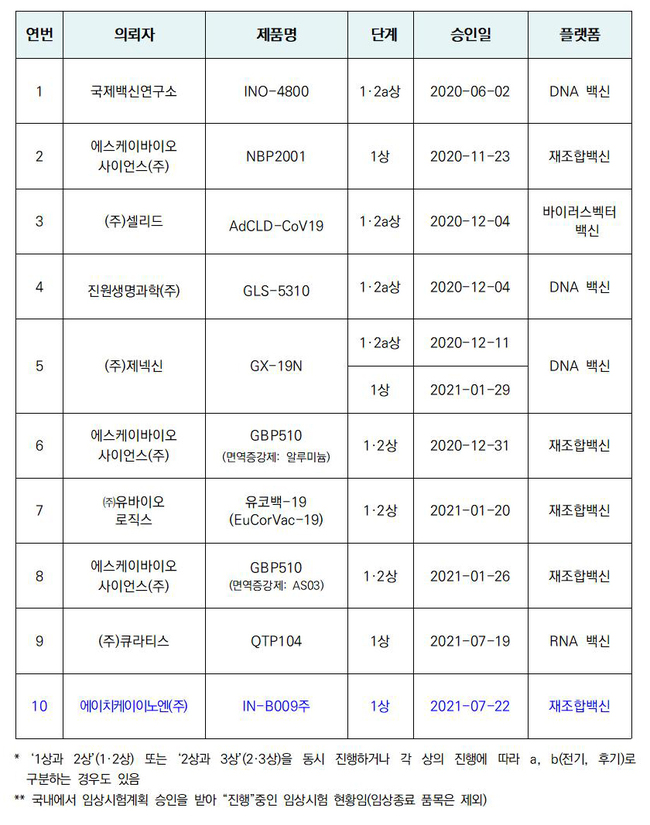 진행 중 코로나19 백신 임상시험 현황(2021.07.22.기준)
진행 중 코로나19 백신 임상시험 현황(2021.07.22.기준)
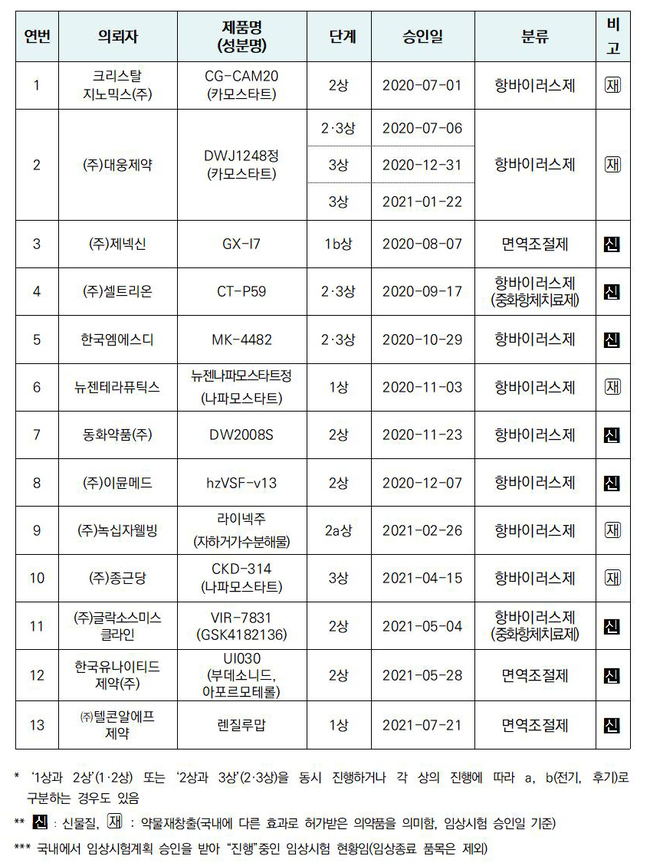 진행 중 코로나19 치료제 임상시험 현황(2021.07.22.기준)
진행 중 코로나19 치료제 임상시험 현황(2021.07.22.기준)